《2022年高中化學 第一章 第3節(jié) 第1課時 原電池的工作原理 化學電源課時作業(yè) 魯科版選修4》由會員分享����,可在線閱讀�,更多相關《2022年高中化學 第一章 第3節(jié) 第1課時 原電池的工作原理 化學電源課時作業(yè) 魯科版選修4(5頁珍藏版)》請在裝配圖網(wǎng)上搜索���。
1�、2022年高中化學 第一章 第3節(jié) 第1課時 原電池的工作原理 化學電源課時作業(yè) 魯科版選修4
一����、選擇題(本題包括7小題,每小題6分���,共42分)
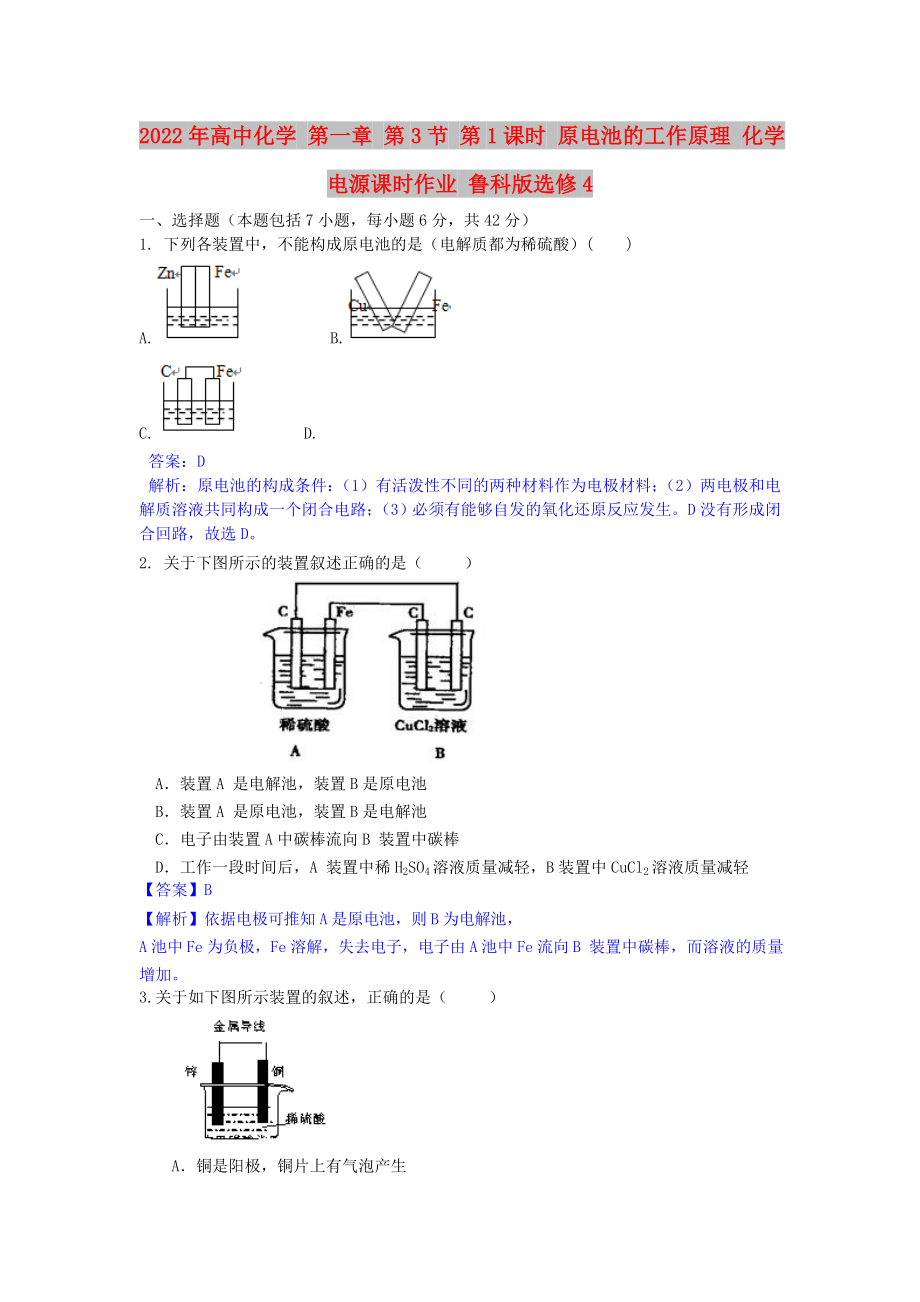
1. 下列各裝置中����,不能構成原電池的是(電解質都為稀硫酸)( )
A. B.
C. D.
答案:D
解析:原電池的構成條件:(1)有活潑性不同的兩種材料作為電極材料�����;(2)兩電極和電解質溶液共同構成一個閉合電路��;(3)必須有能夠自發(fā)的氧化還原反應發(fā)生�。D沒有形成閉合回路�,故選D。
2. 關于下圖所示的裝置敘述正確的是(?? )
A.裝置A 是電解池���,裝置B是原電池???????
B.裝
2����、置A 是原電池,裝置B是電解池
C.電子由裝置A中碳棒流向B 裝置中碳棒????
D.工作一段時間后����,A 裝置中稀H2SO4溶液質量減輕,B裝置中CuCl2溶液質量減輕
【答案】B
【解析】依據(jù)電極可推知A是原電池�,則B為電解池,
A池中Fe為負極�,F(xiàn)e溶解,失去電子��,電子由A池中Fe流向B 裝置中碳棒���,而溶液的質量增加����。
3.關于如下圖所示裝置的敘述����,正確的是( )
A.銅是陽極,銅片上有氣泡產(chǎn)生
B.銅片質量逐漸減少
C.電流從鋅片經(jīng)導線流向銅片
D.氫離子在銅片表面被還原
3���、
答案:D
解析:從圖中可以看出這是原電池���,原電池的電極名稱應說是正��、負極�����,故A錯�;而原電池是活潑金屬被消耗��,故B錯�;負極(Zn)的電子經(jīng)導線流向正極(Cu),故電流方向與電子流向相反��,故C錯�����。
4.下列說法中�,正確的是( )
A.構成原電池兩個電極的材料必須是兩種金屬
B.由銅,鋅作電極與硫酸銅溶液組成的原電池中銅是正極
C.電子通過外導線由鋅流向銅����,通過硫酸溶液被氫離子得到放氫氣
D.銅、鋅原電池工作時���,若有13g鋅溶解����,電路中有0.2mol電子通過
答案:B
解析:構成原電池電極的材料也可以是碳棒�,A錯; 原電池中金屬性弱的做原電池的正極�,B正確;電子由鋅流向
4����、銅,H+在銅電極上得電子放出氫氣���,C錯����;銅�、鋅原電池工作時,若有13g鋅溶解����,電路中有0.4mol電子通過��,D錯��。
5.關于鉛蓄電池的說法正確的是( )
A.在放電時���,正極發(fā)生的反應是
B.在放電時,該電池的負極材料是鉛板
C.在充電時���,電池中硫酸的濃度不斷變小
D.在充電時�����,陽極發(fā)生的反應是
答案:B
解析:鉛蓄電池的放電和充電反應為:���,放電過程是原電池原理,充電過程是電解池原理��,選B�。
6.氧化反應和還原反應分別在兩個電極上自發(fā)進行時,便能構成原電池反應���,下列氧化還原反應在一定條件下不能構成原電池反應的是( )
5���、A.2FeCl2+Cl2===2FeCl3
B.Zn+Ag2O+H2O===Zn(OH)2+2Ag
C.Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O
D.2H2+O2===2H2O
答案:C
解析:A����、B����、D項所示反應均為氧化還原反應�����,且氧化劑和還原劑分別屬于不同的物質�,符合題意.C項雖是氧化還原反應,但氧化劑和還原劑均為Na2S2O3�,不合題意。
7. 甲乙兩位同學一起做水果電池的實驗���,測得數(shù)據(jù)如下:
?
甲同學提出的問題���,乙同學解釋不正確的是
?
【答案】C
【解析】水果電池的電壓與電極的材料也有很大的關系,C錯�。
二、非選擇題(本題
6���、包括4個大題���,共58分)
8.Zn-MnO2干電池應用廣泛��,其電解質溶液是ZnCl2-NH4Cl混合溶液�����。
(1)該電池的負極材料是 ��。電池工作時��,電子流向 ?����。ㄌ睢罢龢O”或“負極”)����。
(2)若ZnCl2-NH4Cl混合溶液中含有雜質Cu2+��,會加速某電極的腐蝕�,其主要原因是 。欲除去Cu2+��,最好選用下列試劑中的 (填代號)�����。
a.NaOH b.Zn c.Fe d.NH3·H2O
(3)MnO2的生產(chǎn)方法之一是以石墨為電極����,電解酸化的MnSO4溶液���。陰極的電極反應式是
��。若電解電路中通過2mol電子��,MnO2的理論產(chǎn)
7�、量為 �����。
答案:(1)Zn(或鋅) 正極 (2)鋅與還原出來的Cu構成銅鋅原電池而加快鋅的腐蝕 b
(3)2H++2e-→H2 ,87g
解析:(1)負極上是失電子的一極 Zn失電子有負極經(jīng)外電路流向正極���。
(2)鋅與還原出來的Cu構成銅鋅原電池而加快鋅的腐蝕��。除雜的基本要求是不能引入新雜質����,所以應選Zn將Cu2+ 置換為單質而除去。
(3)陰極上得電子�,發(fā)生還原反應, H+得電子生成氫氣�。因為MnSO4~MnO2~2 e-,通過2mol電子產(chǎn)生1molMnO2,質量為87g�����。
9.燃料電池是使氣體燃料氧化直接產(chǎn)生電流的裝置�,燃料電池的研究是本世紀最具挑戰(zhàn)性的課題之一
8、����。最近有人制造了一種燃料電池,一個電極通入空氣�,另一電極通入丁烷,電池的電解質是摻雜了Y2O3(三氧化二釔)的ZrO2(二氧化鋯)晶體����,它在高溫下能傳導O2-。試回答下列問題:
(1)該電池放電時的化學反應方程式為:
________________________________________________________________________���。
(2)該燃料電池的電極反應式為:
正極:13O2+52e-―→26O2-
負極:2C4H10+26O2--52e-―→8CO2+10H2O
則固體電解質中的O2-向________極移動(填“正”或“負”)��。
(3)某金
9���、屬的相對原子質量為52.00���,用上述電池電解該金屬的一種含氧酸鹽的酸性水溶液時,陽極每放出3 360 mL(標準狀況)氧氣����,陰極析出金屬10.4 g,在該含氧酸鹽中金屬的化合價為________���,在該實驗中,若不考慮能量的損失��,電池中消耗丁烷的質量最少是____________g(結果精確至0.01 g)�。
答案:(1)2C4H10+13O2===8CO2+10H2O (2)負 (3)+3 1.34
解析:(1)2C4H10+13O2===8CO2+10H2O;
(2)根據(jù)電極反應式可知氧離子由正極移向負極�����;
(3)設金屬的化合價為x�,則根據(jù)得失電子守恒關系可得×4=x
所以可得x=
10、3���,故此過程中轉移的電子的物質的量為0.6 mol�����,所以消耗的丁烷的質量為1.34 g���。
10.新型高能鈉�硫電池以熔融的鈉��、硫為電極���,以導電的陶瓷為固體電解質。該電池放電時為原電池�,充電時為電解池,反應原理為:2Na+xSNa2Sx�����。
(1)放電時Na發(fā)生________反應���,S作________極�。
(2)充電時Na所在電極與直流電源的________極相連�。
(3)放電時負極反應為
________________________________________________________________________;
充電時陽極反應為
______________
11、__________________________________________________________����。
(4)用此電池作電源電解飽和NaCl溶液,當陽極產(chǎn)生33.6 L(標準狀況)氣體時�����,消耗金屬Na的質量為______�。
答案: (1)氧化 正 (2)負 (3)Na-e-―→Na+ S-2e-―→xS (4)69 g
解析:該題考查化學“兩池”(原電池、電解池)的原理及應用����,以新的科技成果即新型高能鈉�硫電池為背景,要求考生學會應用原電池的原理解釋新問題��、新現(xiàn)象�����。主要考查對知識的應用能力����、計算能力�����、推理能力等。解答本題要仔細審題��,尋找突破口——“電池放電時為原電池”��,根
12����、據(jù)原電池的知識,失電子�,發(fā)生氧化反應的電極是負極;得電子�,發(fā)生還原反應的電極是正極。(1)Na作負極�,S作正極。負極反應為Na-e-―→Na+��;(2)“充電時為電解池”�,根據(jù)電解的知識,陽極失電子��,發(fā)生氧化反應���;陰極得電子��,發(fā)生還原反應���。因此Na所在的電極是陰極����,與直流電源的負極相連���,S所在的電極是陽極�����,與直流電源的正極相連�����,陽極反應式為
S-2e-―→xS�����。(4)電解飽和NaCl溶液陽極產(chǎn)生的氣體是Cl2,由2Cl--2e-―→Cl2����,又2Na-2e-―→2Na+,可列式求得Na的質量為69克。
11.依據(jù)氧化還原反應:2Fe3+(aq)+Fe(s) = 3Fe2+(aq)���,設計原電池并
13�����、完成如圖所示實驗�。
請回答下列問題:
(1)電極X的材料是??????? ???? ��;石墨電極為電池的??????????? 極����。
(2)B裝置中發(fā)生的電極反應方程式為?????????? ?;(2分)表面皿中溶質Na2SO4的作用是 �。
(3)銅絲b與濾紙接觸處的現(xiàn)象為______________________;此處電極反應方程式為_________________��。
答案:(1)鐵 正 (2)Fe3++e-=Fe2+ 增強溶液的導電性 (3)濾紙變?yōu)榧t色 O2+2H2O+4e-=4OH-
解析:將2Fe3+(aq)+Fe(s) = 3Fe2+(aq)拆成兩個半反應�,氧化反應Fe-2e-=Fe2+,還原反應F2e3++2e-=2Fe2+��,可知負極材料為鐵���,則X為鐵���,石墨電極為原電池的正極�。銅絲a為陽極���,b為陰極�����,活性電極作陽極����,陰極水中的H+放電生成H2和OH-����。
■反思總結—自我學習評價
□錯題序號xx
□錯因分析及對策
 2022年高中化學 第一章 第3節(jié) 第1課時 原電池的工作原理 化學電源課時作業(yè) 魯科版選修4
2022年高中化學 第一章 第3節(jié) 第1課時 原電池的工作原理 化學電源課時作業(yè) 魯科版選修4