《九年級(jí)化學(xué)上冊(cè) 第五單元 課題1 質(zhì)量守恒定律教案 (新版)新人教版(II)》由會(huì)員分享,可在線閱讀�,更多相關(guān)《九年級(jí)化學(xué)上冊(cè) 第五單元 課題1 質(zhì)量守恒定律教案 (新版)新人教版(II)(2頁(yè)珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索。
1�����、九年級(jí)化學(xué)上冊(cè) 第五單元 課題1 質(zhì)量守恒定律教案 (新版)新人教版(II)
教學(xué)目標(biāo)
知識(shí)與技能
通過(guò)實(shí)驗(yàn)測(cè)定�����,使學(xué)生理解質(zhì)量守恒定律的原因���。
過(guò)程與方法
初步培養(yǎng)學(xué)生應(yīng)用實(shí)驗(yàn)方法來(lái)定量研究問(wèn)題和分析問(wèn)題的能力��。
情感態(tài)度與價(jià)值觀
培養(yǎng)學(xué)生由感性到理性�����,由個(gè)別到一般的認(rèn)識(shí)方法����。
重點(diǎn)
對(duì)質(zhì)量守恒定律涵義的理解和運(yùn)用。
難點(diǎn)
對(duì)質(zhì)量守恒定律涵義的理解和運(yùn)用�����。
關(guān)鍵
通過(guò)自主學(xué)習(xí)和實(shí)驗(yàn)探究總結(jié)定律
教法����、學(xué)法
設(shè)疑,以實(shí)驗(yàn)為導(dǎo)向���,講練結(jié)合��。
課型
新授課
教學(xué)準(zhǔn)備
儀器:托盤天平�����、燒杯�、廣口瓶�、玻璃棒、酒精燈����、氣球、吸管等���。
藥品:白磷��、NaOH溶液��、Cu
2�、SO4溶液����、鐵釘、碎雞蛋殼����、稀鹽酸、石灰水等���。
教學(xué)流程
教師活動(dòng)
學(xué)生活動(dòng)
二次備課
一�、自主學(xué)習(xí)
1、知識(shí)回顧:怎樣正確書(shū)寫化學(xué)式
讓學(xué)生互相出題����,練習(xí)書(shū)寫。
2�、出示學(xué)習(xí)目標(biāo)
明確目標(biāo)??
3、 出示自學(xué)提綱
組織學(xué)生自學(xué)
閱讀提綱�,
學(xué)生自學(xué)得出結(jié)論
質(zhì)量守恒定律
鹽酸與石灰石反應(yīng)前后質(zhì)量的測(cè)定
自主探究
現(xiàn)象:二次質(zhì)量一樣,天平保持平衡
結(jié)論:參加反應(yīng)的物質(zhì)總和等于反應(yīng)后生成物的各物質(zhì)的質(zhì)量總和��。
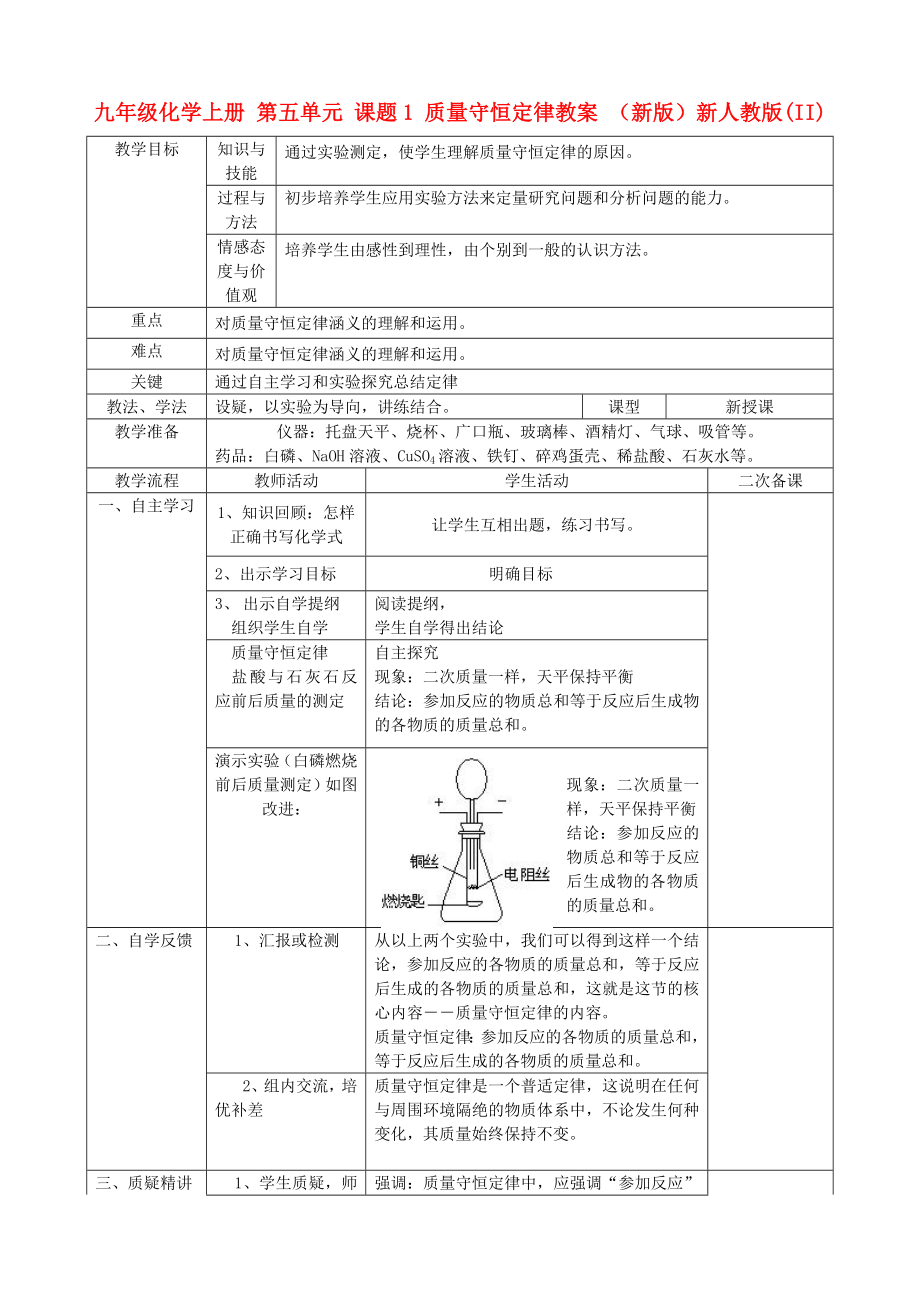
演示實(shí)驗(yàn)(白磷燃燒前后質(zhì)量測(cè)定)如圖改進(jìn):
現(xiàn)象:二次質(zhì)量一樣�����,天平保持平衡
結(jié)論:參加反應(yīng)的物質(zhì)總和
3��、等于反應(yīng)后生成物的各物質(zhì)的質(zhì)量總和����。
二、自學(xué)反饋
1��、匯報(bào)或檢測(cè)
從以上兩個(gè)實(shí)驗(yàn)中,我們可以得到這樣一個(gè)結(jié)論����,參加反應(yīng)的各物質(zhì)的質(zhì)量總和,等于反應(yīng)后生成的各物質(zhì)的質(zhì)量總和�,這就是這節(jié)的核心內(nèi)容--質(zhì)量守恒定律的內(nèi)容���。
質(zhì)量守恒定律:參加反應(yīng)的各物質(zhì)的質(zhì)量總和�����,等于反應(yīng)后生成的各物質(zhì)的質(zhì)量總和���。
2、組內(nèi)交流����,培優(yōu)補(bǔ)差
質(zhì)量守恒定律是一個(gè)普適定律,這說(shuō)明在任何與周圍環(huán)境隔絕的物質(zhì)體系中��,不論發(fā)生何種變化��,其質(zhì)量始終保持不變����。
三��、質(zhì)疑精講
1����、學(xué)生質(zhì)疑����,師生共同解疑
強(qiáng)調(diào):質(zhì)量守恒定律中,應(yīng)強(qiáng)調(diào)“參加反應(yīng)”和“質(zhì)量總和”����。
2、教師橫向拓展和縱向
4���、挖掘
為什么物質(zhì)在化學(xué)反應(yīng)前后����,各物質(zhì)的質(zhì)量總和會(huì)相等呢��?
在化學(xué)反應(yīng)過(guò)程中�����,只是參加反應(yīng)的各物質(zhì)的原子重新組成而生成其它物質(zhì)的過(guò)程,也就是說(shuō)�����,在一切化學(xué)����,反應(yīng)前后,原子的種類沒(méi)有改變�,原子的個(gè)數(shù)沒(méi)有增減��,原子的質(zhì)量也沒(méi)有變化�,所在,化學(xué)反應(yīng)前后�����,各物質(zhì)的質(zhì)量總和是相等的���。
四�、總結(jié)提高
1�、出示精選習(xí)題
蠟燭在燃燒時(shí),越燒����,蠟燭越短����,質(zhì)量也就越小�����,說(shuō)明它不適合質(zhì)量守恒定律����,對(duì)嗎?為什么���?
這種說(shuō)法不對(duì)��,因?yàn)橄灎T時(shí)�����,反應(yīng)物是蠟燭的氧氣�����,而產(chǎn)物為二氧化碳?xì)怏w和水蒸氣�,產(chǎn)物都以氣體形式散逸到空氣中,所以越燒��,質(zhì)量越輕�����,它還適合質(zhì)量守恒定律的�。
2、總結(jié)歸納
總結(jié)全節(jié)內(nèi)容�����,突出理解質(zhì)量定恒定律�。
3�、作業(yè):課堂
課后練習(xí)1、2����、3
家庭
課后練習(xí)4
板書(shū)設(shè)計(jì)
第物單元 化學(xué)方程式
課題1 質(zhì)量守恒定律
一、內(nèi)容:參加化學(xué)反應(yīng)的各物質(zhì)的質(zhì)量總和等于反應(yīng)后生成的各物質(zhì)的質(zhì)量總和���。
二���、原因:化學(xué)反應(yīng)前后原子的種類���、數(shù)目和質(zhì)量均沒(méi)有改變。
教后記
 九年級(jí)化學(xué)上冊(cè) 第五單元 課題1 質(zhì)量守恒定律教案 (新版)新人教版(II)
九年級(jí)化學(xué)上冊(cè) 第五單元 課題1 質(zhì)量守恒定律教案 (新版)新人教版(II)