《《從鋁土礦到鋁合金》(從鋁土礦中提取鋁教學(xué))課件:課件七(13張PPT)》由會(huì)員分享���,可在線閱讀����,更多相關(guān)《《從鋁土礦到鋁合金》(從鋁土礦中提取鋁教學(xué))課件:課件七(13張PPT)(13頁珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索��。
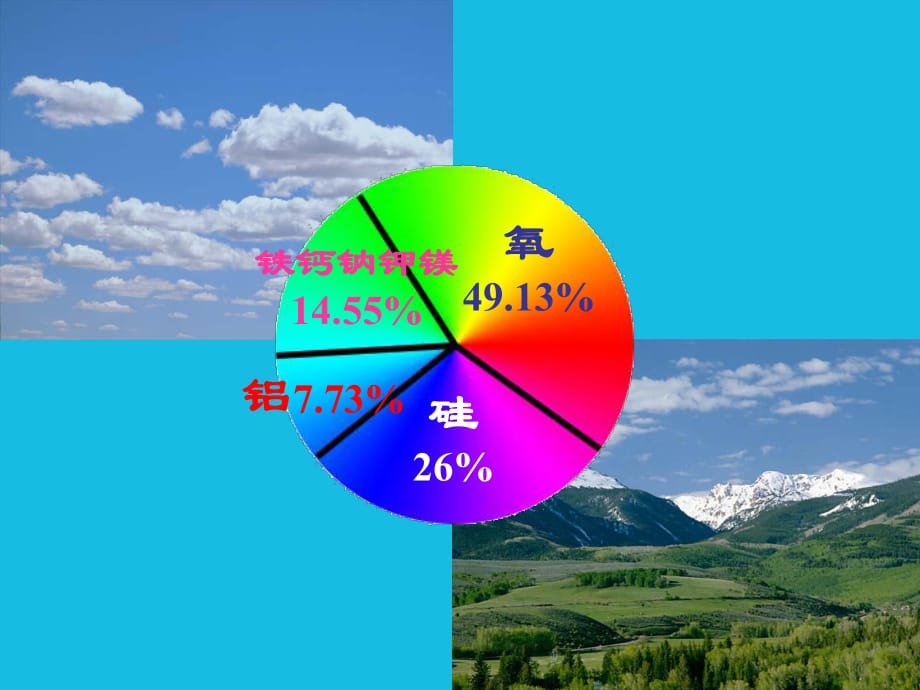
1�����、氧49.13%硅26%鋁 7.73%鐵 鈣 鈉 鉀 鎂14.55% 鋁 及 其 合 金 的 應(yīng) 用 鋁 的 冶 煉 史w 傳 說 拿 破 侖 三 世 的 刀 叉 具 是 用 鋁 制 造 的 ���。 筵 席上 ��, 他 為 多 數(shù) 客 人 提 供 金 餐 具 �, 而 只 讓 少 數(shù) 客人 使 用 鋁 餐 具 , 是 為 了 讓 用 鋁 餐 具 的 客 人 留 下更 深 刻 印 象 ����。w 1885年 , 在 美 國 首 都 華 盛 頓 特 區(qū) 落 成 的 華 盛 頓紀(jì) 念 碑 上 的 頂 帽 也 是 用 金 屬 鋁 制 造 的 �����。w 因 為 在 19世 紀(jì) ���, 鋁 是 一 種 珍 貴 的 金 屬 ���。 人
2、 們 最初 得 到 的 鋁 粒 如 同 珍 寶 �����, 它 的 價(jià) 格 同 黃 金 相 當(dāng) ���。因 為 從 鋁 礦 石 中 把 鋁 提 煉 出 來 , 是 極 其 困 難 的 ��。 w 1884年 ���, 在 美 國 奧 伯 林 學(xué) 院 化 學(xué) 系 �����, 有 一 位 叫做 查 爾 斯 馬 丁 霍 爾 的 青 年 學(xué) 生 ���。 當(dāng) 時(shí) 他 只有 二 十 一 歲 ��。 一 次 �����, 他 聽 一 位 教 授 說 : “ 不 管誰 能 發(fā) 明 一 種 低 成 本 的 煉 鋁 法 �, 都 會(huì) 出 人 頭地 ��。 ” 這 使 霍 爾 意 識(shí) 到 只 有 探 索 廉 價(jià) 的 煉 鋁 方法 �, 才 能 使 鋁 被 普 遍 應(yīng) 用
3、�����。w 霍 爾 采 用 瓷 坩 堝 ��, 碳 棒 ( 陽 極 ) 和 自 制 電 池 ����,對(duì) 氧 化 鋁 �, 即 精 制 的 氧 化 鋁 礦 進(jìn) 行 電 解 ����。 1886年 2月 的 一 天 , 他 終 于 看 到 小 球 狀 的 鋁 聚 集 在 陰極 上 ��。 霍 爾 此 時(shí) 異 常 激 動(dòng) ���, 帶 著 他 第 一 次 獲 得的 一 把 金 屬 鋁 球 去 見 他 的 教 授 ��。 后 來 ���, 這 些 鋁球 竟 成 為 “ 王 冠 寶 石 ” , 至 今 仍 珍 存 在 美 國 制鋁 公 司 的 陳 列 廳 中 �。w 廉 價(jià) 煉 鋁 方 法 的 發(fā) 明 , 使 鋁 這 種 在 地 殼 中 含 量約 占
4��、 8%的 元 素 ���, 從 此 成 了 為 人 類 提 供 多 方 面 重要 用 途 的 材 料 。 而 發(fā) 明 家 霍 爾 ����, 當(dāng) 時(shí) 還 不 滿 23周 歲 �。 那 么 ,霍 爾 是 如 何 用 氧 化 鋁 得到 鋁 的 呢 ? 從 鋁 土 礦 中 提 取 鋁 一 ����、 氧 化 鋁 的 性 質(zhì)w 1、 物 理 性 質(zhì) 白 色 難 熔 的 固 體 物 質(zhì) �, 難 溶 于 水 。w 2����、 化 學(xué) 性 質(zhì) (1)與 酸 反 應(yīng) : Al2O3+ 3H 2SO4 = Al2(SO4)3+3H 2O (2)與 堿 反 應(yīng) : Al 2O3+2NaOH = 2NaAlO2 +H 2O兩 性 氧 化 物 :
5、既 能 與 酸 反 應(yīng) 生 成 鹽 和 水 ����, 又 能 與 堿 反 應(yīng) 生 成 鹽 和 水 。 天然氧化鋁剛玉紅寶石(Al 2O3)藍(lán)寶石(Al2O3) 二 �����、 從 鋁 土 礦 中 提 取 鋁 的 過 程 和 原 理w 閱 讀 教 材 P62,圍 繞 下 列 問 題 討 論 �, 并 寫 出 有 關(guān) 反 應(yīng) 方 程式 ,是 離 子 反 應(yīng) 的 寫 離 子 方 程 式 。w ����、 用 NaOH 溶 液 溶 解 鋁 土 礦 的 目 的 是 什 么 �? w 2�����、 為 什 么 Al2O3能 溶 解 在 NaOH 溶 液 中 �, 而 Fe 2O3卻 不能 ? 這 說 明 了 Al2O3和 Fe 2O3的 化
6�����、 學(xué) 性 質(zhì) 是 否 相 似 ����?w 3、 向 過 濾 后 的 的 所 得 溶 液 中 通 入 過 量 CO 2后 �����, 除 了 得到 Al( OH ) 3沉 淀 外 ����, 濾 液 中 主 要 成 分 是 什 么 ? AlO2- Al(OH)3 偏 鋁 酸 鹽 與 弱 酸 的 轉(zhuǎn) 化 2NaAlO2 + 3H 2O + CO2 = 2Al(OH )3 + Na2CO3( 少 量CO2) NaAlO2 + 2H 2O + CO2 = Al(OH )3 + NaH CO3(過 量 CO2)Al(OH ) 3不 會(huì) 溶 于 弱 酸 �。 AlO2- Al(OH)3 偏 鋁 酸 鹽 與 強(qiáng) 酸 的 轉(zhuǎn) 化 NaAlO2 + H 2O + H Cl = Al(OH )3 +NaCl Al(OH )3會(huì) 溶 于 強(qiáng) 酸 作 業(yè) : 67面 1、 2���、 8
 《從鋁土礦到鋁合金》(從鋁土礦中提取鋁教學(xué))課件:課件七(13張PPT)
《從鋁土礦到鋁合金》(從鋁土礦中提取鋁教學(xué))課件:課件七(13張PPT)